|
1 脓毒症的发病机制
1.1 肠道细菌/内毒素移位
1.2 受体与信号传导通路的激活与抑制
1.3 炎症平衡失调与细胞凋亡及免疫麻痹
1.4 “晚期介质”――高迁移率族蛋白-1的参与
1.5 凝血功能障碍
1.6 神经-内分泌-免疫网络调节失衡
1.7 基因多态性等
2. 脓毒症的微循环障碍微循环侧流暗场(SDF),旁流暗场(SDF)障碍在脓毒症的进展中起重要作用
2.1 微循环障碍可导致和加重MODS
2.2 重度脓毒症的一些临床指标的特点都是继发于微循环改变的,比如低血压、低血管阻力、低灌注压等
2.3 大体血压正常时就可能发生局部灌注不足,因此早期检测微循环侧流暗场(SDF),旁流暗场(SDF)障碍是比较困难的
3 脓毒症时的微循环侧流暗场(SDF),旁流暗场(SDF)特点
3.1 微循环是脓毒症病理生理改变的关键场所
3.2 多种因素会影响到微循环网络:3.3 血流重新分布
3.4 内皮细胞激活和损伤
3.5 上皮细胞失去多糖保护屏障
3.6 微血管渗透性增加,导致水肿和血容量减少
3.7红细胞变形能力降低,毛细血管阻塞
3.8白细胞粘附力增加并其变形力降低,加重毛细血管阻塞
3.9白细胞活性增强,直接破坏微循环(侧流暗场(SDF),旁流暗场(SDF))结构、细胞间相互作用及凝血功能
3.10 DIC的发生
3.11 动脉平滑肌张力及其对血管活性物质的敏感性增加,继而NO产生增多
3.12 功能性毛细血管密度(指单位面积上开放流动的毛细血管数)下降
四、 床旁微循环的检测 1. 微循环侧流暗场(SDF),旁流暗场(SDF)结构和功能的监测在脓毒症诊断和疗效评价中起重要作用2.
近年来,新的影像学技术正交偏振光谱(OPS)成像和旁流暗场(SDF)成像,可以使我们在床旁观察微循环侧流暗场(SDF),旁流暗场(SDF)图像 。
五、 OPS和SDF 二者原理基本相同,SDF优于OPS:1.
正交偏振光谱(OPS)成像对光线过于敏感,容易造成模糊影像从而影响对毛细血管的观察;OPS需要具备高能光源 2.
旁流暗场 (SDF)成像是对OPS技术的改进,已用于临床观察微循环侧流暗场(SDF),旁流暗场(SDF)状态。
六、 重度脓毒症的危险分层
近年来,提出的器官衰竭评分(SOFA)和 PIRO评分能更直观地解决研究中病人的选择与分层这个复杂的问题。
七、 器官障碍/衰竭评分
1994年, Vincent JL制定的脓毒症相关的(后更名为序贯性的)器官衰竭评分(SOFA),
SOFA最高评分以及SOFA
delta评分(SOFA最高评分减去入ICU时SOFA评分,或住ICU期间器官衰竭的增加程度),后2个评分系统在全球范围内被证明能更好地说明或预测ICU患者的预后。例如John
Marshall提出的多器官功能障碍评分(MODS),Jean-Roger Le Gall提出的Logistic
器官功能障碍(LOD)评分。这些评分系统均基于相似的原理,JL
Vincent总结如下: 1. 器官衰竭并非简单的全或无现象,而是从器官功能轻微改变至完全衰竭的连续性过程 2.
器官衰竭并非是一个静止的过程,在疾病的发展过程中器官功能障碍的程度随时不断变化 3.
为了便于对任何ICU中的任何病人进行评分,用于评估器官功能的指标应该是客观、简单且实用的,但也应该是可靠的、每个医院均能常规检测,并且对受累脏器是特异性的.目前,于哪个评分系统是最佳的,或如何最佳地使用某一评分系统尚无统一的意见。
<BR>但是,所有被广泛应用的评分系统都包括6个主要脏器/系统(心血管、呼吸、血液、中枢神经、肾脏和肝脏)。采用生理指标(如PaO2)和治疗指标(如血管活性药物应用)进行评价。主要差别在于评价心血管衰竭的方法不同:SOFA采用血压和升压药的支持水平;MODS采用压力校正性心率(心率×中心静脉压/平均动脉压),而LOD采用对心率和收缩压进行评分。MODS
评分:呼吸系统――氧分压与吸入氧浓度比值(PaO2/FiO2)
肝脏系统――血清总胆红素浓度
肾脏系统――血清肌酐浓度
心血管系统――压力调整的心率〔pressure adjusted heart rate, PAHR, PAHR =
心率×右房压(或中心静脉压)/平均动脉压〕血液系统――血小板计数
,神经系统――格拉斯哥昏迷评分(GCS)评分每个系统都有4 分,总分为0~24分。 MODS
评分与患者院内病死率及存活患者住ICU 的时间呈正相关关系,评分的器官系统中未将胃肠道包含在内,反映心血管系统的指标――压力调整的心率(PAHR)需要监测中心静脉压,且要经过复杂的计算,在实际应用中有所不便,不利于在急诊开展。MODS
评分对MODS患者的预后预测相对APACHEⅡ、SAPSⅡ等更准确,但是在重症脓毒症侧流暗场(SDF),旁流暗场(SDF)病人动态评分来评估病情中还不如APACHE
Ⅱ,说明评分系统存在适用范围。有建议将MODS评分和APACHEⅡ评分联合应用,较两种评分系统单独应用更能提高对急诊内科并发MODS的危重患者预后的预测价值,感染相关的器官衰竭评分系统(
sepsis-related organ failure assessment , SOFA)
SOFA评分最初用于描述感染导致的MODS患者(成人)的发生、发展过程,评价病情和预测死亡率。后通过对ICU
混合患者的前瞻性研究表明, SOFA 评分还可用于全身性感染患者以外的其他患者, 故SOFA也可
称为序贯器官衰竭估计。评分包括呼吸、血液、肝脏、心血管、神经和肾脏6个器官系统,每个器官系统含1~2个变量,按功能损害程度分别计0~4分,总分为0~24分。患者的病死率随着每一脏器的SOFA评分的升高而上升。
SOFA 评分与Marshall的MODS 评分相比更侧重于早期、动态监测MODS病程的变化和演变过程。在心血管系统变量的选择上,SOFA
评分为低血压,较 MODS 评分的PAHR更简单、易行,适用于临床和急诊。 SOFA
评分不足之处是①缺乏对胃肠道功能的判断②评分最初为ICU患者设计,是否适用于急诊
内科病人,有待进一步验证;③对预后的预测不够准确。急诊脓毒症侧流暗场(SDF),旁流暗场(SDF)死亡率评分(mortality in emergency
department sepsis, MEDS)
随着拯救脓毒症侧流暗场(SDF),旁流暗场(SDF)运动(SSC)的开展,进一步要求急诊科医生能够快速准确的诊断脓毒症患者的病因、评估病情严重程度(包括死亡风险)、并给予及时合理的治疗。
前面提到的评分系统可用于各种危重症病人,但并没有考虑到急诊科脓毒症侧流暗场(SDF),旁流暗场(SDF)患者的特点。2003年Shapiro等人针对急诊感染患者提出了急诊脓毒症死亡率(MEDS)评分,通过对3179名18岁以上存在可疑感染的急诊患者28天入院死亡率的研究,在24项可能与死亡率有关的变量中挑选出九项组成MEDS评分。
根据患者死亡风险分级,将评分分为五级:极低危险组(0~4分)、低度危险组(5~7分)、中度危险组(8~12分)、高度危险组(13~15分)、极高危险组(大于15分)。
<BR>在此项研究从极低危险组到极高危险组的死亡率为1.1%~39%,说明MEDS评分的分值越高,患者的死亡率越高,
此评分系统可以评价病情程度和预测死亡率,有助于临床的治疗。 <BR>在对感染患者的评估上MEDS评分比 REMS评分和MEWS评分表现更佳。与原降钙素(PCT)联合应用,可增加对急诊脓毒症侧流暗场(SDF),旁流暗场(SDF)患者死亡率预测的准确性
。
MEDS评分是第一个被用来对脓毒症自然病程全程进行检验的急诊评分系统,对于符合炎症反应综合症(SIRS)的急诊患者同样可以准确预测28天死亡率,但有研究表明,在对143名重度脓毒症和脓毒症侧流暗场(SDF),旁流暗场(SDF)休克的急诊患者应用MEDS评分并不能准确预测死亡率。近期一项回顾性研究应用APACHEⅡ、SAPSⅡ、MEDS和MPMⅡ四种评分方法对246名重度脓毒症患者入院死亡率进行预测比较后发现,MEDS评分表现最差。有学者认为,MEDS评分适用于那些怀疑有脓毒症的早期患者,而不适用于重度脓毒症或脓毒症侧流暗场(SDF),旁流暗场(SDF)休克的患者。
因为最初用于MEDS评分研究的人群是那些怀疑有感染的患者,这类患者的死亡率小于10%,而重度脓毒症和脓毒症休克的患者死亡率在35%。有报道称MEDS评分可以有效的用于重度脓毒症的患者,并较APACHEⅡ评分表现更佳。可见,对于MEDS评分的使用需要更广泛的、多中心的前瞻性研究,增加样本的数量,并避免回顾性研究对结果的影响。
PIRO系统由 John Marshall参照肿瘤TNM分级系统设计的。根据易感因素(Predisposition)、打击
(Insult)、机体反应 (Response)及伴发的器官功能不全 (Organ
dysfunction),对脓毒症侧流暗场(SDF),旁流暗场(SDF)患者进行危险分级诊断PIRO系统首先在2000年10月第五次多伦多脓毒症会议上提出的;2001年脓毒症及相关术语的国际定义大会上被采纳,PIRO系统虽然很有意义,但是至今为止仍然仅是概念上的。2004年,第一次报道了一个关于PIRO系统的小样本临床实验2008年,Moreno
等报道了一个由多个国家共同完成的多中心的大样本临床实验(SAPS 3-PIRO),目的是检验改良的PIRO系统(使用诱因、感染和器官功能障碍/衰竭的概念)是否对ICU中严重感染、脓毒症侧流暗场(SDF),旁流暗场(SDF)和脓毒性休克患者的死亡率有预测作用。经过多参数分析,被证明有意义的参数如下:诱因(Box1):年龄、从什么地方转入ICU的、并发症、入ICU前的住院时间(天)、入ICU的原因感染(Box2):院内获得性感染、感染的范围(局部或扩散)、感染的部位及病原菌反应(Box3):肾功能障碍、凝血障碍;心血管、呼吸、肾脏、凝血及中枢神经系统的功能衰竭,根据这些参数对预后的影响,制定了一个评分表,并且得出与SAPS
3 PIRO评分相关的出院时状况的公式: logit=-46.6757+ln(PIRO+76.7688) ×
9.8797院内死亡率可用以下公式计算:死亡率=elogit/(1+ elogit)最后得出结论,在总体人群及特定人群中,
PIRO评分系统对脓毒症病人的预后有良好的预测作用。
八、 脓毒症相关性脑病
SAE是由于感染引起的全身反应而导致的脑功能障碍,而且必须临床或实验室排除中枢神经系统的直接感染。
脓毒症引起的意识改变最先报道于斑疹伤寒的病人,但是各种病原菌包括革兰氏阳性、阴性细菌、病毒、真菌和寄生虫都可以引起这种变化
。最开始把脓毒症引起的意识改变定义为脓毒症性脑病(septic
encephalopathy),但是由于这一概念是脓毒症(侧流暗场(SDF),旁流暗场(SDF))的一种状态,包含中枢神经系统的直接感染(如脑炎和脑膜炎),而非仅指由身体产生的细胞因子、炎症因子作用于脑引起的脑功能障碍,所以现在常用的概念已经变迁为SAE。随着ICD10的出版,其中脑病(encephalopathy)的诊断已经被谵妄(Delirium)所取代,所以现在亦有学者主张将SAE变更为脓毒症相关性谵妄(Sepsis
Associated Delirium,SAD) 。由于当前世界上大多数学者对于这种疾病的诊断仍然在使用SAE的概念,所以本文亦将使用SAE的概念。在美国,每年脓毒症(侧流暗场(SDF),旁流暗场(SDF))的发病率约为240例/10万,死亡率约为20%-30%,尤其在ICU,死亡率可以高达50%以上。在美国,脓毒症的发病率在过去的20年中稳步上升,每年约上升1.5%,这与SAE发病率的上升是一致的。
<BR>
基于不同的临床标准,脑电图(EEG)标准和体感诱发电位(SEP)的测定,SAE发病率的区别很大,从8%至71%。Sprung等人将脑病定义为急性意识状态的改变,并收集了1333例脓毒症病人,分析后发现其中23%出现了脑病;脑病病人的死亡率(49%)高于先前就存在脑功能障碍(41%)和正常意识状态(26%)的病人,但是三组间的血培养却没有显著的差异。当格拉斯哥评分(GCS)从15分降至8分以下时,SAE的死亡率会由16%升高至63%。虽然,SAE还不是一个判断预后的独立因素,但是,脓毒症(侧流暗场(SDF),旁流暗场(SDF))确实会导致危重症病人脑病的发生,出现SAE的脓毒症(侧流暗场(SDF),旁流暗场(SDF))病人的死亡率是增加的。
SAE的病理生理学
(1)脑内信号传导系统:脑部内稳态的保持需要中枢神经系统和中枢免疫系统处于平衡状态。脑免疫系统的活化可以被视为脑内感觉系统信号在脑内的扩散,这种脑对信号的感受主要通过以下三个途径:a通过迷走神经b通过脑室周围器官(CVOs)c通过活化的内皮细胞。迷走神经可以通过其轴突上的炎症因子受体感受外周炎症的刺激,传入神经纤维将免疫相关信息传送至延髓孤束核而刺激下丘脑垂体肾上腺轴,然后传出神经在网状内皮系统释放乙酰胆碱通过单核细胞上的尼古丁样胆碱能受体抑制炎症反应,抑制细胞活化和细胞因子释放。这就是所谓的胆碱能抗炎途径。脑室周围器官缺乏血脑屏障的保护,是血、脑之间信息直接交流的结构,它们包绕着松果体、联合下器和穹窿下器,特别是中隆起神经垂体和终板血管器处的血管,这些是下丘脑、垂体中心和最后区的一部分,接近于脑干的自主调节神经核团。脑室周围器官本身具有免疫成分,如Toll样受体、CD14、和肿瘤坏死因子α的受体,并具适应表达性,通过这些受体血源性的细胞因子汇进入脑,对神经内分泌和自主神经中枢有激动作用。内皮细胞的活化会导致脑的炎症和神经毒素递质的释放,加强脑部炎症反应的扩散。
脑内炎症因子的作用
:活化的中性粒细胞、单核细胞释放致炎炎症因子如白细胞介素1α(IL-1α)、IL-1β,IL-6
和肿瘤坏死因子α(TNF-α)。IL-1刺激迷走神经传入纤维后会依次影响脑干、边缘系统、下丘
脑,而引起“病态行为”,包括活动减弱,食欲减退、情绪低落和认知能力下降。IL-1β刺激位
于部分脑室周围器官的脑核团,这些结构的活化会改变位于杏仁核和下丘脑边缘系统的功能,而造成情绪低落和厌食。高水平的IL-6可能与氨基酸代谢有关,使血中支链氨基酸减少。TNF-α会改变脑内色氨酸的代谢,使4-羟基喹啉(可转变为有神经毒素作用的喹啉酸)增加和5-羟色胺减少。这些生物化学的改变会导致情绪的低落。
在SAE中BBB遭到破坏,循环中致炎炎症因子和微生物产物如LPS会进入到脑中,引起脑CD40、CD14(LPS的受体)和内皮细胞粘附因子的表达
。一旦炎症发生,这种活化的信号就会播散到控制行为反应、神经内分泌和自主神经功能的脑区域,并影响胶质细胞(微小胶质细胞、星形胶质细胞、少突胶质细胞)和神经元,引起免疫受体和各种炎症介质表达。
Alexander Jacob等人的动物实验发现,在内毒素血症(侧流暗场(SDF),旁流暗场(SDF))时补体C3上升,而CR1-related y(Crry,一种膜辅因子蛋白调节补体级联反应影响补体经典途径和选择途径)下降。LPS依赖补体上调iNOS,在内毒素血症可以使AQP4(由星形胶质细胞终足和活化的微小胶质细胞表达的一种水通道蛋白,控制脑水量)表达增加,增加脑水含量。
BBB通透性的改变和微血管功能障碍:广泛的血管内皮细胞活化被看做是脓毒症(侧流暗场(SDF),旁流暗场(SDF))休克的标志
。LPS和致炎细胞因子可以引起人脑微血管内皮细胞上E选择素、细胞内粘附因子-1、血管粘附因子-1和CD40的表达。他们也能激活编码环氧化酶-2的基因使其复制,使iNOS过度表达而增加BBB的通透性。脑内皮细胞虽然不能表达CD14,但是LPS能通过可溶的CD14触发内皮细胞的促分裂原活化蛋白激酶的级联反应。LPS激活的内皮细胞表达TNF-α、IL-1的受体;
表达iNOS。继脑部炎症反应之后,这些依赖内皮细胞信号机制产生的炎症介质继续作用于周围的脑细胞。内皮细胞的活化会导致BBB的破坏,通透性增加。
另外,星形胶质细胞对于维持神经元的平衡状态起着重要作用。星形胶质细胞的损伤影响局部血流的调节,使局部突触的活动减弱,并引起BBB的功能障碍。血管内皮细胞的活化也可以引起脑血管的功能障碍,使血管紧张度、凝血功能发生改变,导致出血和缺血的发生。
氧化应激,线粒体功能障碍和细胞凋亡:脓毒症(侧流暗场(SDF),旁流暗场(SDF))的病理生理学机制之一是氧化应激。氧化应激会影响细胞的功能和活力。LPS和细胞因子可以活化星形胶质细胞并上调iNOS,氧和精氨酸在一氧化氮合成酶作用下通过减少NADPH产生一氧化氮和超氧化物。这些反应在杀灭病原菌的同时会激发宿主细胞的氧化应激反应。一氧化氮与超氧化物作用形成过氧化氮,过氧化氮会抑制线粒体的呼吸功能和糖酵解酶导致脑部能量供应的减少。
氧化应激反应最主要的结果是引起细胞的凋亡。凋亡是细胞程序性死亡的过程,可能由于TNF-α刺激神经元上受体所触发。细胞凋亡的另外一个可能机制是线粒体损伤。
脓毒症(侧流暗场(SDF),旁流暗场(SDF))会使身体处于持续严重分解状态。肌肉组织可分解为支链氨基酸和芳香族氨基酸,芳香族氨基酸经过肝脏代谢,而支链氨基酸为肌肉提供能量。在脓毒症病人和动物模型中可以见到脑脊液和血浆中芳香族氨基酸上升速度较支链氨基酸快。这种改变可以出现在多器官衰竭之前,这可能与脓毒症(侧流暗场(SDF),旁流暗场(SDF))时肝代谢功能受损和清除功能下降有关。Basler等人发现脑病病人血浆中芳香族氨基酸浓度与血浆降钙素原(PCT)和IL-6浓度有关。PCT、IL-6浓度越高,氨基酸代谢异常越明显。在SAE中,神经递质的失衡也起重要作用。γ-氨基丁酸(GABA)是抑制性神经递质,Minuk等人发现厌氧菌、需氧菌都可以使血浆GABA浓度升高;Rocio
Serantes等人发现IL-1β通过磷脂酰肌醇-3-激酶/Akt途径使GABA细胞膜受体上调;支链氨基酸和芳香族氨基酸的失衡增加前脑和脑干的氨基丁酸能受体。神经递质的改变可以减少存在5羟色胺能和去甲肾上腺素能系统的脑部的糖利用。LPS可以减少海马锥体神经突触的神经递质,使神经元兴奋性下降,影响行为和情绪系统。在脓毒症(侧流暗场(SDF),旁流暗场(SDF))时血浆和脑脊液中酪氨酸、色氨酸、苯丙氨酸
浓度上升,会减少神经递质合成。
SAE的诊断
临床特征:SAE是一种新发生的意识改变,并且必须具备全身炎性反应
综合征(SIRS)或脓毒症(侧流暗场(SDF),旁流暗场(SDF))(Sepsis)的症状,这种意识的改变包括:定向障碍、焦虑、思维混乱、嗜睡、昏睡、甚至昏迷,焦虑和嗜睡可以交替出现
。诊断SAE必须排除其他原因引起的意识改变,如中枢神经系统的直接感染、脑创伤、脑卒中、脂肪栓塞、代谢方面和药物方面等。震颤、扑翼样震颤、肌阵挛通常见于代谢性脑病,颅神经异常通常不常见于SAE。偏瘫在SAE中可以见到,但必须进一步排除其他原因,如脑卒中。ICU中的病人可以出现各种各样脑病,
SAE是十分常见的,尤其在脓毒症(侧流暗场(SDF),旁流暗场(SDF))病人中发病率可达50%至70%。为了防止上机病人情绪紧张,对呼吸机不耐受,拔出气管插管,所以镇静药物可适当应用,但是镇静药物的应用会影响意识状态的评估。
ICU中,如何判断病人是否可能存在SAE呢?
脑损伤的血清生物学标记物:神经元特异性烯醇化酶(NSE)和星形胶质细胞蛋白S100B是评价脑功能障碍的有力指标。NSE持续高水平状态可能反应脑部的炎症反应和神经元的坏死。星形胶质细胞蛋白S100B是酸性的钙结合蛋白二聚体,反应胶质细胞损伤,其升高可以反应脑受损程度。有研究表明,S100B水平越高,APACHEⅢ评分越差,ICU病人死亡率越高。而且以S100B0.65ug/l和NSE16.7ug/l为界点可以预测早期死亡率
。
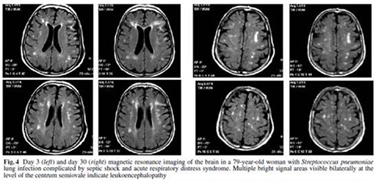
影像学: SAE的脑CT无特异性表现,而脑MRI表现却十分引人注意,因为它可提供更多信息。Sharshar对9例脓毒症(侧流暗场(SDF),旁流暗场(SDF))休克合并神经系统急性改变患者,5例病人FLAIR像灌注像双侧脑白质呈高强度损害,2例DWI像呈多发高强度损害,另外2例脑MRI正常。
EEG: EEG对SAE患者灵敏度高,特异性差。Young 等人对SAE脑电图变化进行研究,在脓毒症(侧流暗场(SDF),旁流暗场(SDF))早期,可无异常,随着病情加重,EEG表现为过度的Theta波,显著的Delta波,三相波,最后表现为抑制或爆发抑制。根据EEG异常程度分为5级,发现病人死亡率与EEG异常级别有直接关系。正常EEG患者死亡率为零。过度的Theta波为19%,显著的Delta波为36%,三相波为50%,抑制或爆发抑制为67%。
BIS、SEP:BIS评分除可评价脑功能外,还可更好的评价意识状态,今后可能成为评估脓毒症(侧流暗场(SDF),旁流暗场(SDF))病人危重程度的重要指标。在SIRS出现前4小时,SEP波幅就开始减小,所以此指标可成为SIRS病人脑功能障碍的敏感指标,但操作繁琐性可能制约其应用。
SAE的治疗
目前,SAE无特效治疗方法。应该积极控制感染。包括外科清除脓肿,恰当应用抗生素。但是,由于细菌的耐药性,抗生素起效慢,杀灭细菌后,细菌释放炎症刺激原增加等原因,抗生素治疗效果SAE效果并不理想。
多种原因可以活化胶质细胞,上调致炎炎症因子导致细胞坏死。所以,阿片样物质受体拮抗剂(调节微小细胞活化)、抑制TNF产生药物、减少微小胶质细胞产生NO的药物、抑制微小胶质细胞活化药物、抵抗炎症效应药物等,都被应用于抑制上述途径,以达到治疗SAE目的,但其效果有待进一步证实。
由于iNOS在SAE中起重要作用,所以其抑制剂被应用于治疗SAE。虽然iNOS抑制剂可以减少LPS导致的细胞凋亡,但是并没有改善脓毒症(侧流暗场(SDF),旁流暗场(SDF))鼠的意识状态,而且会加重脑缺血,增加心血管系统并发症。
由于氨基酸的失衡是SAE可能发病机制之一,所以有人应用高浓度支链氨基酸治疗SAE。Freund用此方法成功治疗5例SAE病人。
脓毒症(侧流暗场(SDF),旁流暗场(SDF))会导致氧化应激的发生产生大量活性氧族,使细胞功能发生障碍。所以抗氧化剂也被应用于治疗SAE。抗坏血酸作为抗氧化剂可以减少活性氧族的产生,可以减少脓毒症(侧流暗场(SDF),旁流暗场(SDF))鼠的死亡率
,可以抑制iNOS的诱导作用;抗坏血酸可以保护星形胶质细胞,清除谷氨酸盐,保护神经元。
另外,活化蛋白C有抗炎作用,也可应用治疗SAE,但其效果还没有得到大规模临床试验证实。镁离子有保护血脑屏障的功能,减少通透性,减轻脑水肿。联合血浆滤过吸收(CPFA)可以清除炎症因子和炎症介质,抑制全身炎症反应,进而影响血脑屏障通透性。
新争议:乳酸清除率或中心静脉血氧饱和度?
复苏目标中推荐使用中心静脉血氧饱和度(ScvO2)或混合静脉血氧饱和度(SvO2)来评估组织“输氧”和耗氧量的平衡情况,然而这一单中心试验成果自2001年发表之后,医学界对其就有不少争议。最近有研究发现,对于监测ScvO2在时间、技术和专业器械方面的要求是实施EGDT
的主要障碍。
美国Jones等进行了一项前瞻性、多中心、随机对照临床试验,结果发现,脓毒症(侧流暗场(SDF),旁流暗场(SDF))休克EGDT复苏目标,将中心静脉(上腔静脉)和平均动脉压维持在标准水平(ScvO2≥70%),另外采取措施控制乳酸清除率(维持血清乳酸清除率≥10%),与控制ScvO2的治疗方案相比,患者院内死亡率没有统计学差异
<BR>但相对于ScvO2的监测而言,乳酸清除率的测定方法更简单易行且对机体侵扰较小。
我们期待出现更多此类设计优质、研究深入的临床试验,为EGDT的科学有序发展提供更高质量的依据。临床施行脓毒症(侧流暗场(SDF),旁流暗场(SDF))早期复苏:任重而道远。虽然,目前已有越来越多的研究证据支持脓毒症(侧流暗场(SDF),旁流暗场(SDF))早期复苏核心策略对急诊科及ICU内患者具有显著益处,但临床工作中的实际情况是对该策略的实施与执业严重不足,早期治疗策略所代表的强化、优先、积极的治疗理念并未获得医护人员的普遍贯彻,进而已影响到患者受益的幅度。
国内外的研究已开始关注此类问题,美国曾组织过对急诊科医护人员进行调查问卷,实施脓毒症(侧流暗场(SDF),旁流暗场(SDF))复苏过程中的三大主要障碍是:
1. 护理人员缺乏。2. 监测中心静脉压的技术困难 。3. 早期鉴别脓毒症患者的困难 4. 治疗策略实施的依从性不高,原因:
5. 现有的诊断手段不足限制了严重脓毒症(侧流暗场(SDF),旁流暗场(SDF))及其并发症的早期诊断 6. 临床医师业务熟悉程度不高 7. 对SSC指南的知晓程度不高
8. 对实施集束化治疗策略具体措施的顾虑等
可见,除了治疗策略自身仍有待完善之外,医护人员的配置及培训、教育与实践也是脓毒症(侧流暗场(SDF),旁流暗场(SDF))早期复苏中的重要一环。同时我们还应该看到,每一项疾病治疗指南的颁布和修订都是一个漫长而曲折的过程,需要人们付出更多的智慧和努力来完成这一过程。而且,不可盲目地强调指南的权威性,在临床工作中医护人员必须切实结合患者的个体差异以期望得到最佳的治疗效果。
文章来源:http://www.365heart.com/show/80252.shtml |